本文提出了 FDIF (Formula-Driven supervised learning with Implicit Functions),一种基于隐式函数(SDF)的 3D 医学图像分割预训练框架。该方法完全利用数学公式生成合成数据和标签,实现了在无真实数据、无专家标注情况下的 SOTA 性能。
TL;DR
在 3D 医学图像分割领域,FDIF (Formula-Driven supervised learning with Implicit Functions) 提出了一种革命性的思路:彻底抛弃真实医疗数据进行预训练。通过数学公式定义的隐式函数(SDF),FDIF 能够无限量地生成具有复杂几何结构和真实纹理的合成 3D 卷,并自带精准标注。实验证明,这种完全“凭空捏造”的预训练效果,竟然能比肩在数万例真实病例上训练的自监督模型。
痛点深挖:为什么以前的合成数据“不好用”?
在医疗 AI 领域,数据的“围墙”极高:隐私合规严苛、医生标注昂贵。
此前虽然有 PrimGeoSeg 等基于公式驱动的研究,但其局限性在于:
- 几何单一性:基于体素的挤压(Extrusion)生成方式,难以模拟带有空腔、孔洞等复杂拓扑的解剖结构。
- 纹理缺失:由于体素是离散的,缺乏到物体边界的连续距离信息,导致合成的图像强度分布机械、死板,无法体现医疗影像中的组织异质性和边缘特征。
方法论详解:SDF 的魔力
FDIF 的核心直觉在于将物体建模为连续的 有向距离函数 (Signed Distance Functions, SDF)。在这一框架下,任何一点到表面的距离都是已知的,这为精细化的纹理控制提供了数学基础。
1. 三位一体的函数库
- SDF 库 (几何之源):包含 109 种植入公式的几何体,通过布尔运算、旋转和平滑融合,可以组合出无穷无尽的复杂形状。
- 位移函数 (DF) 库 (表面细节):利用 Pseudo-Perlin 噪声、锯齿波等干扰 SDF 场,在原本光滑的几何体表面生成“肿瘤结节”或“血管壁”般的微观细节。
- 映射函数 (MF) 库 (影象强度):将 SDF 的距离值映射为 CT/MRI 的原始像素强度(Intensity)。例如,通过指数衰减函数模拟组织内部的密度变化。
2. 算法流程
算法首先在 3D 网格中随机采样多个基元,通过位移函数增加纹理,再通过映射函数生成强度。最巧妙之处在于标签分配:在物体重叠区域,通过“小物优先”的策略解决遮挡问题,生成像素级精准的标签地图。
 图 1:FDIF 的核心设计逻辑,从数学公式到复杂的 3D 合成图像。
图 1:FDIF 的核心设计逻辑,从数学公式到复杂的 3D 合成图像。
实验与结果:比肩 SSL 的“人造”性能
研究团队在 AMOS(腹部多器官)、ACDC(心脏)和 KiTS(肾脏肿瘤)三个重磅基准上验证了 FDIF。
核心战绩:
- 超越先辈:在 nnUNet Primus-M 架构下,FDIF 的平均 Dice 分数达到 88.65%,相比同门前辈 PrimGeoSeg 的 86.07% 有显著跨越。
- 对标真实数据:在使用 ResEnc-L 架构时,FDIF (88.70) 甚至小幅超越了在真实大规模脑部 MRI 上预训练的 MAE (88.30)。
- 跨任务通用性:预训练后的模型在 3D 分类任务上也表现优异,平均准确率提升了 1.32%。
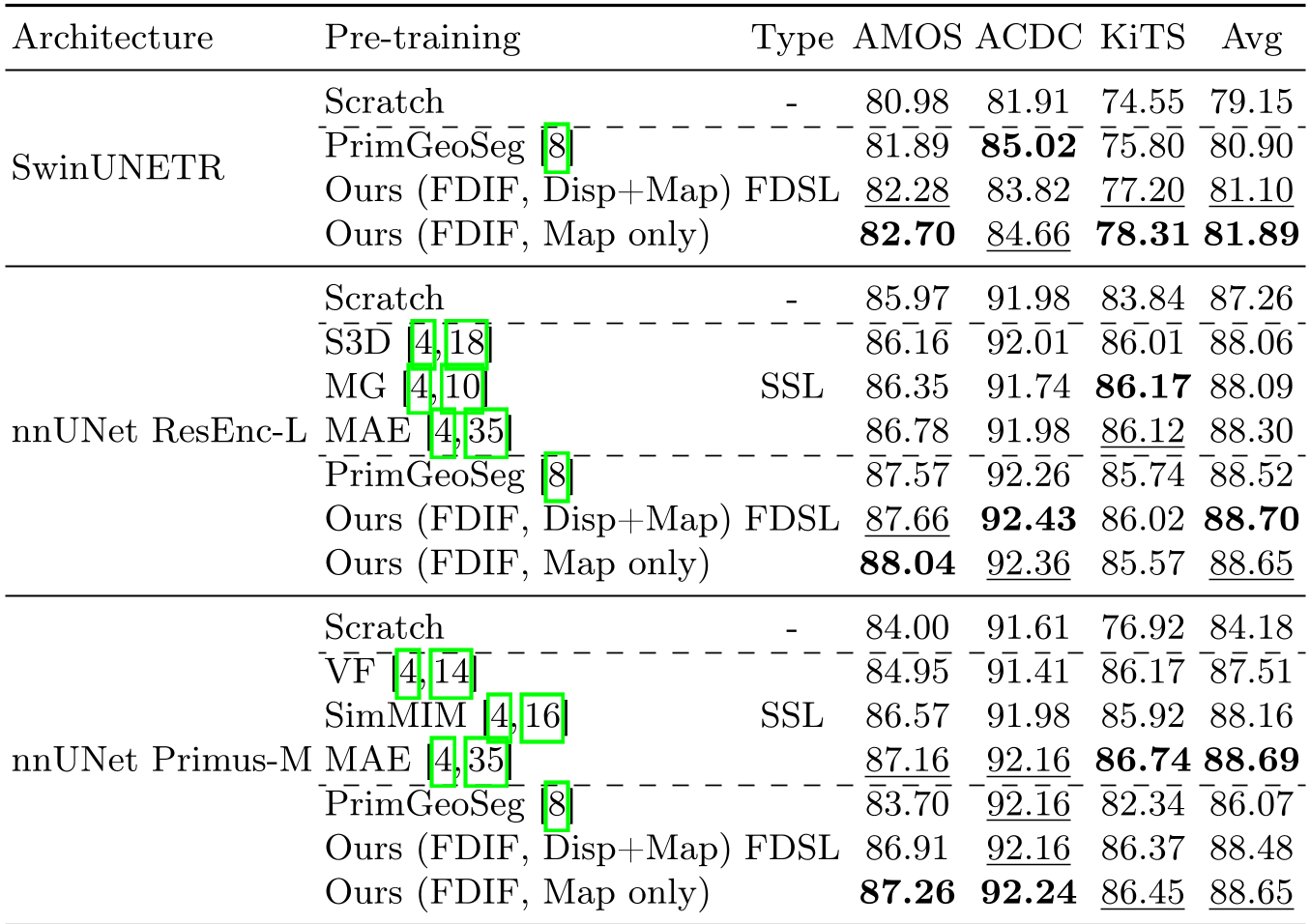 表 1:FDIF 与自监督学习(SSL)及其他基准在不同架构下的分割性能对比。
表 1:FDIF 与自监督学习(SSL)及其他基准在不同架构下的分割性能对比。
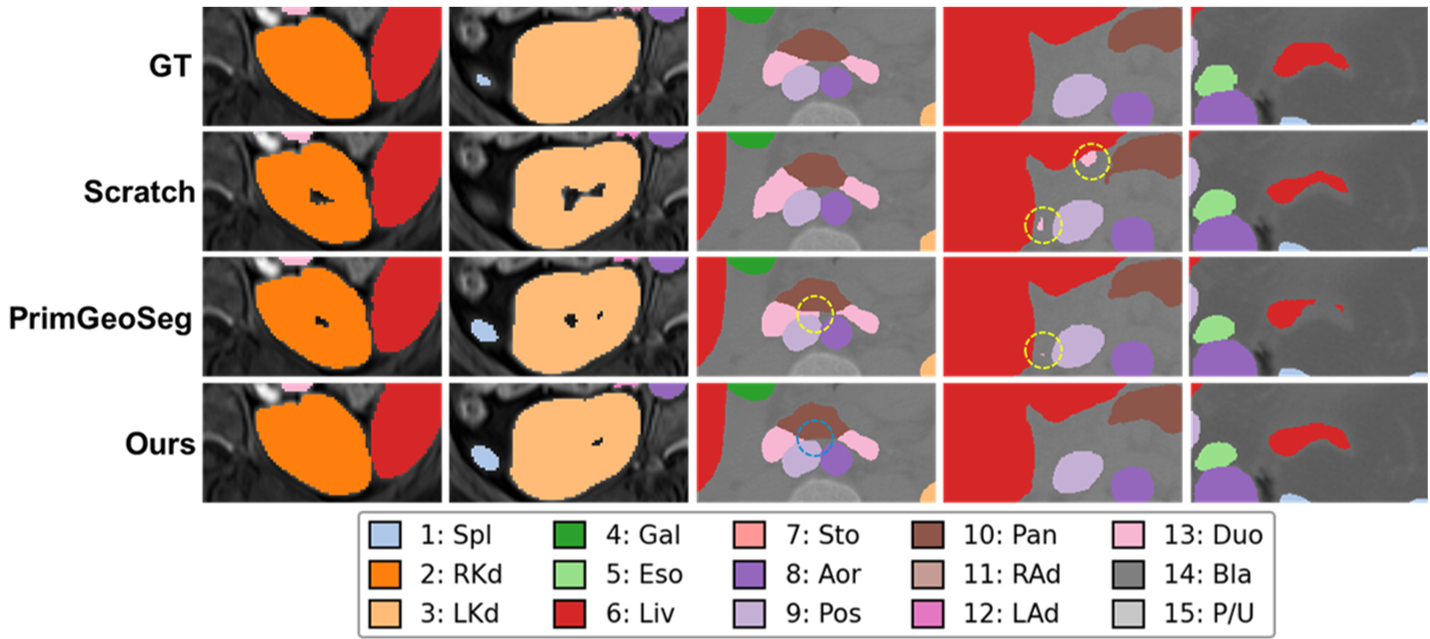 图 2:定性可视化显示,FDIF 能够有效减少漏检和过检测,特别是在复杂的腹部器官边缘。
图 2:定性可视化显示,FDIF 能够有效减少漏检和过检测,特别是在复杂的腹部器官边缘。
深度洞察与总结
为什么 FDIF 能起作用? 作者通过消融实验发现,纹理多样性对表征学习的贡献远大于单纯增加几何类别的数量。这暗示了深度网络在分割医学影像时,对局部纹理模式的敏感度极高,而 SDF 恰恰提供了模拟这种敏感度的最佳手段。
局限性与展望
尽管 FDIF 在分割任务中表现亮眼,但在某些特定的分类任务(如 MedMNIST Nodule)中甚至不如从零训练(Scratch)。这说明目前的函数库虽然丰富,但对某些极端细微且具有高度特定生物学意义的特征(如结节微小钙化)捕捉仍有不足。
启示:未来的研究或许可以将 FDIF 与 Foundation Models(如 SAM 系列)相结合,利用隐式函数作为“先验增量”,为超大规模、跨领域的医疗 AI 模型提供源源不断的燃料。
